281
тропосферой, в атмосфере и наблюдается от поверхности Земли до высот 80– 90 км. Воздух в
стратосфере – безоблачной, сухой, холодной области – перемешивается очень медленно по
вертикали и относительно быстро по горизонтали. Поэтому опасные вещества, однажды попавшие
в стратосферу, остаются в ней на долгие годы и легко распространяются вокруг Земли, и тем
самым загрязнение стратосферы приобретает глобальные масштабы.
Озон выполняет весьма важную роль естественного фильтра, поглощающего губительное для
всего живого коротковолновое ультрафиолетовое излучение Солнца. Концентрация озона
сравнительно небольшая. Если собрать озоновый слой в окружающую земной шар тонкую
оболочку при нормальном атмосферном давлении, то толщина ее составит всего около 3 мм.
Распределение озона в атмосфере зависит от сезона, активности Солнца, широты места,
техногенного воздействия и т. п. Локальные распределения озона могут отличаться на порядок.
Разрушение озона осуществляется в результате цепной реакции, в которой одна примесная
молекула может разрушить много тысяч молекул озона прежде, чем попадет в более плотные слои
атмосферы и достигнет поверхности Земли вместе с осадками.
Сравнительно недавно схема образования озона в средних слоях атмосферы сводилось всего
лишь к четырем химическим и фотохимическим реакциям с участием только кислородных одно- и
многоатомных частиц (О, О2 и О3). К настоящему времени известно, что для описания
динамического состояния стратосферы необходимо учесть не менее 150 химических реакций.
Химический процесс начинается с поглощения молекулами кислорода О3 ультрафиолетового
излучения. При таком поглощении разрываются химические связи, образуется озон О3
и атомы
кислорода. При попадании моноксида азота NО в атмосферу начинается цепная реакция.
Моноксид азота реагирует с озоном. Образуется диоксид азота NО2, который вступает в реакцию с
атомами кислорода, регенерируя NО. Данные две реакции составляют по существу настоящий
каталитический цикл, в котором NО и NО2 играют роль катализаторов. В таком цикле исчезают
один атом кислорода и одна молекула озона, а соединения азота – NО и NО2
– полностью
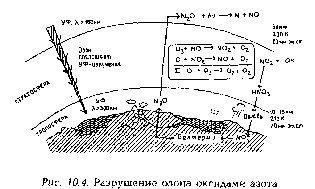
восстанавливаются (рис. 10.4). Предполагается, что рассмотренный каталитический цикл с
участием оксидов азота – главный механизм разрушения озона, в результате которого возникают
озоновые дыры.
Существуют два основных вида источников оксида азота в стратосфере. Первый из них –
естественный – обусловливается бактериями: в природе оксиды азота образуются в основном в
виде N3O при жизнедеятельности почвенных и морских бактерий. Такое относительно инертное
соединение медленно поднимается в атмосфере, где в результате поглощения ультрафиолетового
излучения образуются оксиды азота NО и NO2. Второй источник – различного рода газы
искусственного происхождения, а также газы, образовавшиеся при ядерных взрывах.
С деятельностью человека связан еще один существенный источник загрязнения стратосферы –
галогенпроизводные углерода CFCl3 и CF2Cl3 (хлорфторметаны), широко применяемые в качестве
хладагентов и аэрозольных наполнителей. Данные соединения химически инертны, и какие-либо
вредные воздействия их на живые организмы пока не обнаружены. Однако вследствие той же
инертности они легко поднимаются вверх, достигая стратосферы, где возможен фотолиз под
действием ультрафиолетового излучения. Хлорсодержащие продукты фотолиза Сl и СlО могут
породить свой каталитический цикл, разрушающий озон подобно оксидам азота (рис. 10.5).

